Natürliche Seltenheiten
Alle chemische Elemente außer Lithium, Beryllium und Bor entstanden und entstehen im Universum unter hoher Temperatur, hohem Druck und hoher Dichte durch Kernverschmelzung im Inneren der Sterne (Kernsynthese genannt). Dabei nimmt die relative Häufigkeit der Elemente mit höherer Ordnungszahl Z ab. Da die Ordnungszahl Z im Periodensystem der Elemente der Zahl der Protonen im Atomkern entspricht, kann man also sagen, daß die Häufigkeit der Elemente mit zunehmender Masse abnimmt.
In der Tat ist die Funktion Häufigkeit eines Elementes in Abhängigkeit von der Ordnungszahl Z exponentiell, d.h. leichte Elemente mit weniger Protonen existieren im Universum wesentlich häufiger als schwere Atome (gelbe Hinterlegung in Abb. 1). In diesem Zusammenhang verwundert es nicht, daß Silber (Z = 47, chemisches Symbol Ag) relativ weit rechts und Gold (Z = 79, Au) sehr weit rechts im Diagramm zu finden sind. Mit der Ordnungszahl 83 ist Bismut (Bi) das schwerste noch stabile Element. Ab Z = 84 (Polonium) zerfallen die Elemente nach bestimmten Halbwertszeiten. D.h. nach Gold kommen nur noch vier stabile Elemente, die eine größere atomare Masse aufweisen:

(u = atomare Masseneinheit, 1u = 1,66 * 10-27 kg)
Da die Elemente mit gerader Protonenzahl eine höhere Kernstabilität aufweisen, sind sie jeweils häufiger vorhanden, als ihre unmittelbaren Nachbarn (sog. Harkins"sche Regel [1]). Auch aus diesem Aspekt heraus verwundert es nicht, daß Gold und Silber als seltene Elemente ungerade Protonenzahlen aufweisen. Das Diagramm wird nach seinem "Erfinder" Victor Moritz Goldschmidt auch "Goldschmidt-Diagramm" genannt [2].
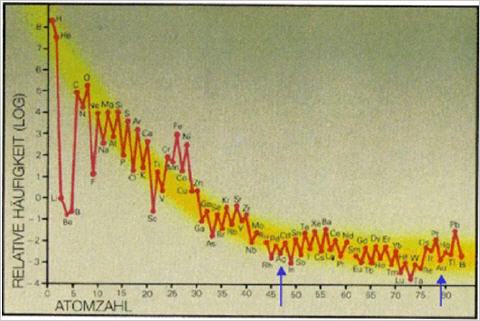
Abbildung 1: Relative Häufigkeit der Elemente im Universum als
Funktion ihrer Protonenzahl, semilogarithmische Darstellung [3];
Silber (Z=47) und Gold (Z=79) sind mit blauen Pfeilen markiert,
Gelbe Hinterlegung verdeutlicht die Exponentialität der Abhängigkeit.
Doch kommen wir aus dem Universum auf unsere Erde zurück. Geologen nennen die oberste Schicht unseres Planeten die "Kruste". Sie ist im Mittel 40 km stark, unter Ozeanen dünner und unter Gebirgen, z.B. dem Himalaya bis zu 70 km stark. Um sich die Größenordnung bzw. Relationen zu verdeutlichen wird gerne das "Apfelmodell" herangezogen. Die Schale eines Apfels entspricht dabei unserer Erdkruste. Die bekannte Zusammensetzung dieser Erdkruste differiert von der oben beschriebenen Zusammensetzung des Universums. Die grundlegenden Regeln wie oben beschrieben gelten jedoch auch hier: Elemente mit hoher Protonenzahl sind seltener. Die genaue Zusammensetzung der Erdkruste können Sie Ref. [1] entnehmen.
Betrachtet man die beschriebene Häufigkeit der (bergbaulich relevanten) Elemente in der Erdkruste mit den bekannten Reserven, so ergibt sich folgender linearer Trendkanal:

Abbildung 2: Reserven wichtiger Metalle in
Abhängigkeit ihrer Häufigkeit in der Erdkruste [4]
Elemente wie Gold, Platin, Blei und Phosphat, die sich am rechten Rand des Kanals befinden, weisen demnach eine hohe relative Reserve auf (relativ bezogen auf ihre eigene natürliche Häufigkeit und relativ im Bezug auf andere Elemente bzw. Metalle); Elemente wie Vanadium, Titan oder Magensium weisen eine niedrige relative Reserve auf.
Mit anderen Worten: Für Elemente, die bereits eine hohe relative Reserve aufweisen, dürfte es ungleich schwerer sein, noch weitere neue und bisher unbekannte Reserven zu finden. Das zuletzt Gesagte gilt vor allem für Gold, wie ein Zitat von V.E. McKelvey vom U.S. Geological Survey aus dem Jahr 1960 verdeutlicht [5]:
"Gold [ist] das am meisten gesuchte Element, dasjenige, von dem die Reserven vermutlich am besten bekannt sind und dessen wirtschaftliche Mindestkonzentration in der Geschichte seines Abbaus und Nutzens am stärksten fiel."
Die wirtschaftliche Mindestkonzentration - engl. "cut-off grade" - ist die minimale Goldkonzentration im Erz, die für einen wirtschaftlichen Abbau notwendig ist. Aufgrund besserer Techniken, so McKelvey, fiel diese Mindestkonzentration für Gold stetig ab.
Es erscheint also logisch und einsehbar, daß es für Minenbetreiber immer schwieriger wird, neue Goldvorkommen zu entdecken, obwohl im Augenblick weltweit fast die Hälfte (!) der Explorationsgelder in die Suche nach dem gelben Metall mit der Protonenzahl 79 investiert wird [6].

Abbildung 3: Weltweite Explorationsbudgets 2007
(1821 Unternehmen, 10 Milliarden US-$) [6]
Zusammenfassend könnte die ableitbare Regel also wie folgt lauten: Investiere in Elemente (Metalle) mit möglichst hoher und ungerader Protonenzahl, die im Bezug auf ihre natürliche Häufigkeit in der Erdkruste bereits eine relativ hohe Reserve ausweisen.
© Jürgen Müller